虽然目前疫苗的接种有效降低了疾病死亡率和传播速率,但治疗药物任然缺乏,且可选性和普及型较差。
由新冠状病毒引发的新型冠状病毒肺炎 (COVID-19)全球大流行为全球公众健康带来了巨大的挑战和影响,也带来了巨大的经济和医疗负担。虽然目前疫苗的接种有效降低了疾病死亡率和传播速率,但治疗药物任然缺乏,且可选性和普及型较差。因此,研发可能具有更高普及型的广谱抗新冠病毒感染的药物具有重要意义。
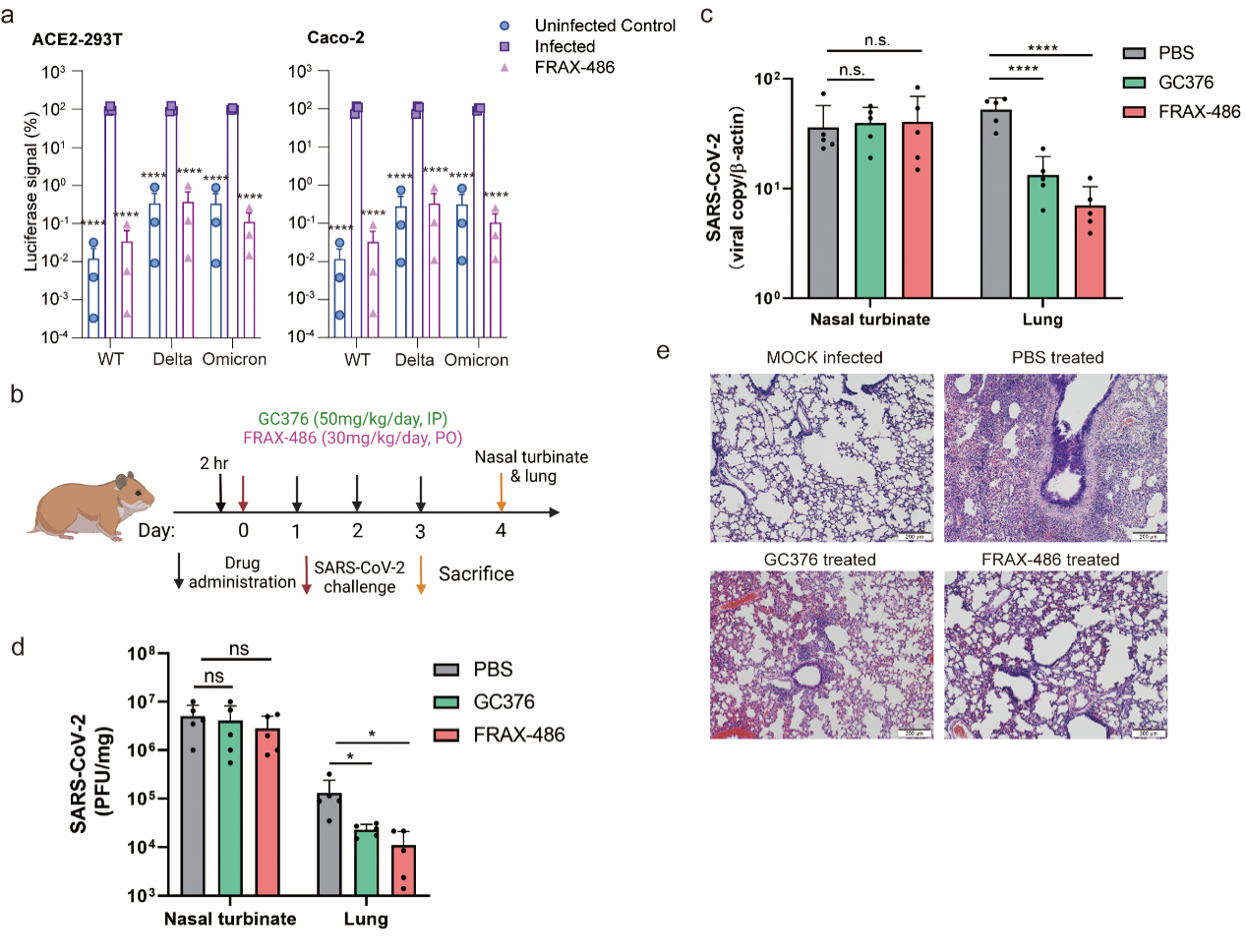
过往研究发现新冠病毒的棘突蛋白可与细胞表面的血管紧张素转化酶2(ACE2)受体相互作用,促进病毒附着和进入细胞,并导致ACE2降解。但是棘突蛋白介导新冠病毒入侵并促进ACE2的降解的分子机制尚不完全清楚。在本研究中,刘明博士等发现棘突蛋白-ACE2通过自噬被细胞内吞和降解,这一过程依赖于网格蛋白介导的内吞作用和PAK1介导的细胞骨架重排。此外,细胞中游离的棘突蛋白则以溶酶体依赖的方式被选择性地裂解为S1和S2亚基。团队还发现,泛PAK抑制剂FRAX-486可以恢复细胞表面的ACE2表达,抑制新冠病毒不同变异株的感染(图1a)。经FRAX-486治疗的仓鼠肺部病毒载量显著降低,肺部炎症明显减轻 (图1b-e)。
本研究得到了香港大学陈福和教授和广州医科大学赵金存教授课题组的大力协助。国家自然科学基金项目(批准号:82000007、82001676、 91842304、82125015、82272337),广东省基础与应用基础研究基金联合基金(批准号:202102020194),广东省钟南山医学基金会(批准号:2020013),香港优配研究金(批准号:17122322)提供了项目资助。
图1. PAK1促进冠病毒入侵细胞和ACE2降解,PAK1抑制剂有广谱抗新冠病毒活性。 a, PAK1抑制剂FRAX-486阻断SARS-CoV-2假病毒变异体(野生型、Delta和Omicron)进入ACE2-293T和Caco-2细胞。b, FRAX-486治疗SARS-CoV-2感染的叙利亚仓鼠模型的体内效果评估示意图。 c-e, FRAX-486降低SARS-CoV-2感染仓鼠肺部的SARS-CoV-2 RNA载量 (c), 病毒滴度(d),降低肺部免疫浸润(e)GC376和PBS分别为阳性对照和阴性对照药物。
Yuxia Zhang
22 October 2023